Глиобластома (мультиформная глиобластома) — наиболее распространенный и агрессивный рак мозга: она составляет более 50% всех первичных опухолей. Глиобластома характеризуется быстрым ростом и часто прорастает в здоровые ткани, что сильно ограничивает доступные варианты лечения. Также большая лекарственных препаратов не проходит через защитный гематоэнцефалический барьер мозга (ГЭБ), что значительно усложняет терапию.
Прогноз глиобластомы неблагоприятный: средняя продолжительность жизни не превышает 15 месяцев с момента постановки диагноза.
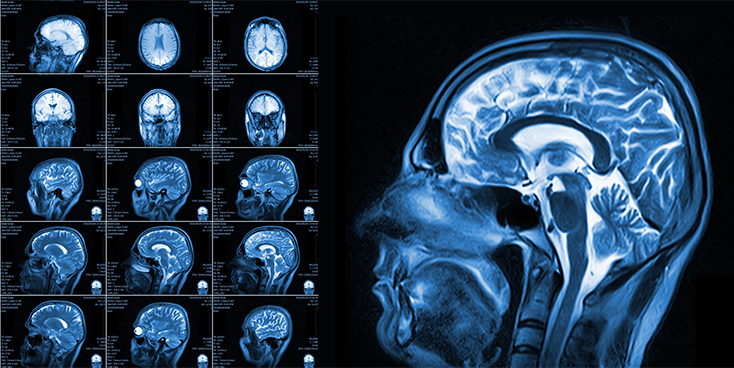
Оперативное лечение глиобластомы
Хирургическое удаление глиобластомы — технически сложная и не всегда осуществимая процедура.
Возможность проведения операции и выбор метода зависят от того, где находится новообразование, какие структуры мозга оно затрагивает, а также от размеров опухоли.
Глиобластомы больших размеров, расположенные в непосредственной близости к жизненно важным центрам мозга, невозможно удалить без повреждения окружающих тканей. Результатом такого вмешательства могут стать пожизненные послеоперационные осложнения — от потери памяти до полного паралича. Также в случае рецидива не всегда удается провести повторное удаление опухоли из-за возможных осложнений.
Химиотерапия при глиобластоме
Несмотря на то, что химиотерапия с использованием препарата темозодала остается основным методом конвенционального лечения, она все равно не увеличивает выживаемость при глиобластоме мозга более чем на 14,6 месяцев после постановки диагноза. Однако хорошая новость заключается в том, что, по данным последних исследований, пациентам с раком мозга можно не прерывать химиотерапию для проведения иммунотерапии: комбинация этих методов даже может повысить выживаемость.
Лучевая терапия при глиобластоме
Лучевая терапия используется как самостоятельный метод лечения после хирургического удаления опухоли или при возникновении рецидива. В основе этого метода — использование энергии электромагнитных излучений для уничтожения быстро делящихся раковых клеток. Но излучение не способно отличать нормальные клетки от опухолевых, что может привести к повреждению здоровой ткани головного мозга. Мы рекомендуем использовать лучевую терапию в комбинации с онколитическими вирусами: она повышает проницаемость защитного барьера головного мозга, и вирусы легче проникают к опухоли.
Иммунотерапия при глиобластоме
Иммунотерапия считается одним из наиболее перспективных направлений в лечении злокачественных новообразований головного мозга, включая глиобластому. Используя конвенциональные методы лечения, такие как хирургическое вмешательство, химиотерапия и лучевая терапия, можно достичь стадии минимальной остаточной болезни, когда в организме останется лишь небольшое количество раковых клеток.
Однако этого недостаточно для полного излечения: опухоль может развиться повторно даже из одной оставшейся в организме раковой клетки. Также клетки новообразования могут приобретать устойчивость к химиотерапевтическим препаратам или лучевой терапии. Поэтому вариантом выбора для пациентов становятся иммунотерапевтические методики, которые предлагают принципиально новую стратегию уничтожения злокачественных клеток.
Онколитические вирусы
Онколитические вирусы — это безопасные для человека вирусные штаммы, которые модифицированы таким образом, чтобы прикрепляться только к раковым клеткам. Вирусы реализуют свое действие благодаря сочетанию двух независимых механизмов. Во-первых, проникая внутрь злокачественной клетки, они размножаются и вызывают апоптоз (запрограммированную гибель клетки). После гибели клетки новые вирусные частицы попадают в системный кровоток, где могут «атаковать» другие раковые клетки.
Во-вторых, вирусы стимулируют собственную иммунную систему пациента бороться со злокачественным новообразованием. Прикрепляясь к раковым клеткам, вирусы как бы делают «помечают» их, делая более узнаваемыми для иммунной системы. Таким образом, «холодные» раковые клетки, ускользающие от иммунных реакций, становятся «горячими».
Мы проводим курс терапии онколитическими вирусами внутривенно или интраназально, но для повышения эффективности сегодня уже доступна новейшая экспериментальная методика — введение онколитического вируса непосредственно в опухоль. Это можно сделать во время операции по удалению глиобластомы или через резервуар Оммайя — устройство с трубкой, ведущей в один из желудочков головного мозга. Внутриопухолевое введение вируса позволяет достигнуть максимального эффекта от лечения. В отличие от внутривенного или интраназального введения, вирусам не приходится преодолевать гематоэнцефалический барьер. Они воздействуют на опухоль напрямую, превращая ее в своеобразную противораковую вакцину. При этом также продолжается выработка новых вирусов, уничтожающих раковые клетки, и стимуляция иммунной системы пациента на борьбу с новообразованием.
Противораковые вакцины
Противораковые вакцины — еще один вид иммунотерапии глиобластомы — учат собственную иммунную систему пациента распознавать опухолевые клетки как «чужие». Так иммунная система пациента сможет атаковать мутировавшие опухолевые клетки, не повреждая здоровые ткани. Каждая вакцина создается индивидуально для конкретного пациента: для этого мы используем образцы опухоли, полученные во время операции по удалению новообразования.
Прогноз при глиобластоме
Прогноз при глиобластоме после удаления также неблагоприятный: пятилетняя выживаемость пациентов не превышает 6,9%. При этом повторные операции и курсы химио-и лучевой терапии плохо переносятся и значительно снижают качество жизни пациентов, влияя на когнитивные и двигательные функции, настроение и работоспособность.
У Biotherapy International большой опыт лечения разных видов рака мозга, включая глиобластому. Более 30 лет назад мы впервые начали применять экспериментальное лечение с использованием онколитических вирусов. С тех пор около десяти наших пациентов полностью вылечились, и достоверно известно, что несколько из них уже более 20-30 лет после терапии живут без рецидивов глиобластомы.
Каждый случай рака уникален, и наша цель — предложить пациентам методы лечения, основанные на последних научных исследованиях, чтоб повысить шансы на излечение от рака мозга даже при самом неблагоприятном прогнозе.
